医疗器械公司注册流程图解
一、前期准备
确定公司基本信息
想好合适的公司名称,要符合医疗器械行业特色且能体现专业性2。
确定真实有效的注册地址,用于接收相关部门信函2。
明确经营范围,例如是生产、销售医疗器械还是提供相关技术服务等。
考虑注册资本数额,虽然现在不需要实际缴纳,但也要合理设定。
准备法定代表人身份证、股东出资比例等基本身份信息和资料。
了解特殊要求
医疗器械行业监管严格,要清楚行业特殊要求,如可能需要办理医疗器械生产许可证或者医疗器械经营许可证等。
确保公司符合医疗器械行业的质量管理体系相关的质量标准和管理要求2。
要保证产品能够符合相关法规要求,以便进行产品的注册和备案,使产品能够上市销售。
二、与代办公司沟通(若选择代办)
若选择像北京中惠万通企业管理有限公司这样的代办公司,会与其详细沟通需求和情况。代办公司会帮您准备注册资料,包括核对公司名称、注册地址、经营范围、注册资本等信息,确保无误。
三、资料提交与审核
提交注册资料
将准备好的资料提交给相关部门。如果是自己办理,要确保资料符合要求;如果是代办公司,他们会凭借与相关部门的关系,快速提交资料,争取高效通过审核。
审核过程
相关部门会对提交的资料进行审核。审核时间根据不同情况而定。
如果审核过程中有任何问题或者需要修改资料,会收到通知并进行相应处理。如果是代办公司,他们会及时与您沟通并协助解决问题。
四、领取营业执照和公章等
审核通过后,可以领取营业执照和公章等物件。如果是代办公司,他们会小心保管并交接到您手上。
五、后续手续办理
税务登记:到税务部门进行登记,以便依法纳税。
银行开户:开设公司银行账户,用于资金往来。
社保开户:为员工办理社保开户手续,依法履行企业的社会保障责任。
六、办理医疗器械相关许可证(根据经营范围)
如果涉及医疗器械生产,需要办理医疗器械生产许可证;如果涉及医疗器械经营,需要办理医疗器械经营许可证。不同类型(一类、二类、三类)医疗器械的许可证办理要求有所不同,要按照相应的法规和流程进行办理。例如:
一类医疗器械:相对低风险,部分手续较为简便,但也要符合相关规定。
二类医疗器械:办公区域和仓库有面积要求,并且需要有专业人员担任质量负责人和质量管理员,还要向省、自治区、直辖市政府药品监督管理部门备案。
三类医疗器械:需要取得生产许可证等相关严格审批的证件。
七、产品注册与备案(如果涉及产品生产销售)
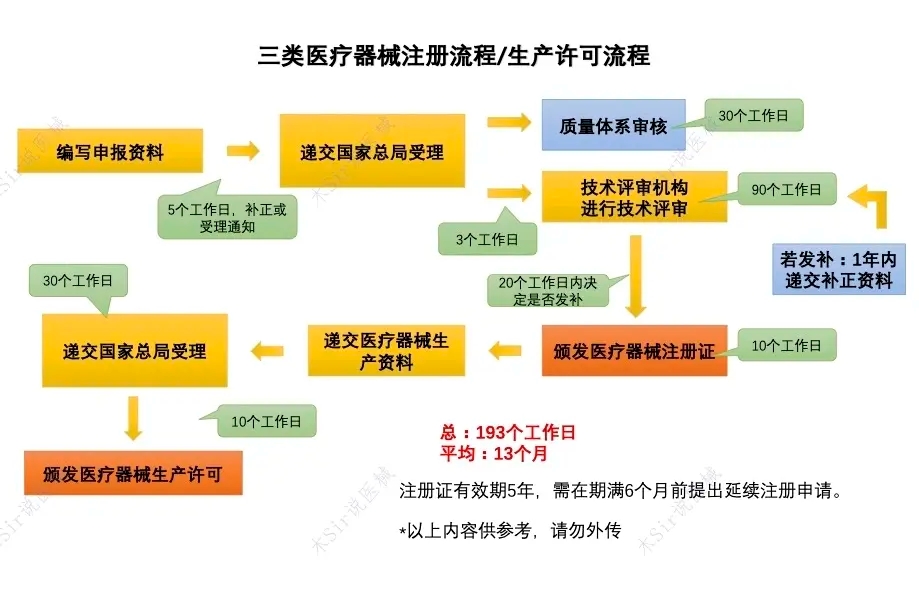
根据医疗器械产品注册流程,对产品进行注册或备案。
界定产品类别
可通过直接搜索标准品名查询分类目录,若无法确定品名,则根据产品描述和预期用途判定。还需查询产品是否需要临床试验,可通过查询国家药监局现行的免临床目录和往期分类界定结果确定。若仍无法确定则进行医疗器械产品的分类界定,确定属于哪一类医疗器械产品,因为不同类别的注册流程和资料要求不同。
产品注册检验
一类医疗器械产品,生产企业可自行出具检测报告,无法自行检测的可委托检测机构检测;二类和三类医疗器械产品需委托国家认可的检测机构检测。企业要提供产品技术要求,检测机构根据技术要求中的参数对产品进行核定,检测机构通常由药监局下属的医疗器械检测所承担,检测合格后,有源医疗器械需要出具电磁兼容报告和全项检测报告,无源医疗器械只需出具全项检测报告,报告封面的CMA标识是注册时药监人员重点关注的内容。注册检验样品生产应符合医疗器械质量管理体系要求,注册检验合格的方可进行临床试验(免临床产品跳过该阶段)。
进行临床试验(免临床产品跳过该阶段)
一类医疗器械产品不需要进行临床试验;二、三类医疗器械产品如果不在国家颁布的医疗器械豁免目录中,或者不能通过与同类产品的信息对比获得临床评价资料,则需要进行临床试验。进行临床试验前要获得药品监督部门的临床备案,筛选合适的临床试验机构并编写详细的临床试验方案,经伦理机构会议审议通过后正式开始临床试验,要招募足够数量的样本,临床试验过程中需要临床协调员和临床监查员全程跟进,项目结束后出具临床评价报告。
建立生产体系
根据《医疗器械生产质量管理规范》的要求,一二三类医疗器械在注册前都必须建立符合规范的GMP生产质量体系,主要包括文件资料、人员场地的合理分配以及产品生产质量的要求,考核通过后通知药品监管部门进行现场审查,建议从建厂之初就介入此过程,生产体系阶段和注册资料递交阶段可同步进行。
注册资料递交及发补
完成临床试验后可提交产品注册资料,申请人应按照相关要求向省食品药品监督管理部门提交申报资料。技术审评机构会在规定工作日内完成第二类、第三类医疗器械的注册技术审评工作(二类医疗器械60个工作日,三类医疗器械90个工作日)。
领取医疗器械注册证
受理注册申请的食品药品监督管理部门在技术审评活动结束后20个工作日之内做出决策,如果产品满足安全性和有效性要求,将给予注册许可,并在作出审批决定后的10个工作日内向申请人发放医疗器械注册证书,并将核准的产品技术要求以附件的形式发送给申请人。











